
   |
|
КНИГИ ПО ХИМИИ: |
|
|
Алкилированием называют реакции, приводящие к замещению водорода гидроксильной, карбоксильной или аминогруппы на алкильную группу.
В настоящем разделе рассматриваются лишь реакции алкилирования гидроксильной группы, приводящие к образованию простых эфиров. Реакции алкилирования карбоксильной группы, приводящие к образованию сложных эфиров, даны в разделе "Реакции ацилирования".
Простые эфиры могут быть получены в результате отщепления молекулы воды от двух молекул спирта путем нагревания его с концентрированной серной кислотой:
R-OH + HO-R а R-O-R + H2O
Данный способ на является, однако, общепринятым. Концентрированная серная кислота при нагревании может разрушать многие органические вещества или вступать с ними в реакцию с образованием сульфокислот и других продуктов. Кроме того, этот способ мало пригоден для получения смешенных эфиров, так как при нагревании с серной кислотой смеси двух спиртов образуется смесь трех эфиров:
R-OH + HO-R' а R-O-R' + H2O
R-OH + HO-R а R-O-R + H2O
R'-OH + HO-R' а R'-O-R' + H2O
Более общим способом превращения гидроксильных соединений в простые эфиры является взаимодействие алкоголятов с галоидными алкилами:
R-ONa + R'I а R-O-R' + NaI
Замещение водорода гидроксильной группы на алкильную группу легко может быть произведено также действием диалкилсульфата в присутствии щелочи:
R-OH + R2SO4 + NaOH а R-O-R' + NaR'SO4 + H2O
При взаимодействии этилового спирта с серной кислотой образуется этилсерная кислота и вода:
C2H5-OH + HO-SO3H а C2H5-O-SO3H + H2O
При температуре 140-150° этилсерная кислота вступает в реакцию с избытком спирта, в результате чего образуется диэтиловый эфир и серная кислота:
C2H5-O-SO3H + HO-C2H5 а C2H5-O-C2H5 + HO-SO3H
Легколетучий диэтиловый эфир отгоняется, увлекая с собой и воду, выделяющуюся при образовании этилсерной кислоты. Поэтому серная кислота не разбавляется водой и сохраняет способность вступать во взаимодействие с новыми количествами спирта, выполняя роль катализатора.
При более высокой температуре (170°) этилсерная кислота разлагается с образованием этилена:
CH3-CH2-O-SO3H а CH2=CH2 + HO-SO3H
Теоретически, при соблюдении надлежащей температуры реакции, можно было бы данным количеством серной кислоты превратить в эфир неограниченное количество спирта. Однако на практике невозможно избежать небольшой затраты серной кислоты на окислительные процессы, сопровождающиеся образованием сернистого газа.
Реактивы: 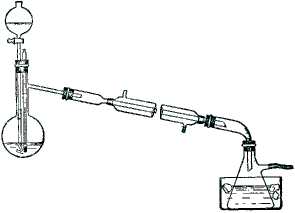 В перегонную колбу емкостью 200 мл берут 30 мл спирта и осторожно, хорошо перемешивая, приливают 30 мл концентрированной серной кислоты. Колбу закрывают пробкой, в которую вставлены капиллярная воронка и термометр, шарик термометра должен быть погружен в жидкость. К ножке капельной воронки при помощи кусочка резиновой трубки присоединяют стеклянную трубку с оттянутым и загнутым кверху концом, также погруженным в жидкость. Колбу соединяют с длинным, хорошо действующем холодильником, к которому в качестве приемника присоединяют колбу для отсасывания. На боковой тубус последней надевают длинную резиновую трубку для отвода в сторону (под тягу) легко воспламеняющихся паров эфира. Приемник охлаждают водой со льдом (рис. 33).
В капельную воронку наливают спирт (120 мл) и нагревают колбу горелкой через асбестовую сетку. Когда температура смеси достигнет 140°, начинают понемногу приливать спирт, следя за тем, чтобы температура не поднималась выше 150°. Спирт приливают с той же скоростью, с какой отгоняется эфир. Через 45-60 мин. прибавление спирта заканчивают, нагревают смесь еще 5 мин., затем гасят горелку и отъединяют приемник.
Дистиллят, кроме эфира, содержит воду, спирт и сернистую кислоту. Его взбалтывают в делительной воронке с 10%-ным раствором едкого натра, взятым в количестве 1/3 объема полученного дистиллята (для удаления сернистой кислоты). Отделив раствор едкого натра, эфир (для удаления спирта) обрабатывают насыщенным раствором хлористого кальция; раствор последнего берут в количестве, равным половине объема дистиллята.
Тщательно отделив водный слой, переливают эфир в сухую склянку и сушат хлористым кальцием (около 10 г), оставляя стоять не менее 4-5 час. Затем перегоняют эфир из перегонной колбы, собирая фракцию, кипящую в пределах 33-38°.
Выход около 40 г.
Темп. кип. чистого эфира 35,6°; уд. вес
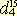 0,7197; показатель преломления 0,7197; показатель преломления 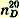 1,3538. 1,3538. При работе с эфиром нужно соблюдать большую осторожность, помня, что эфир сильно летуч и легко воспламеняется. При перегонке эфира следует пользоваться баней с горячей водой; баню нагревают в стороне от прибора и горелку под колбой не зажигают; для поддержания нужной температуры в баню добавляют горячую воду.
Реакция образования изоамилового эфира при нагревании изоамилового спирта с концентрированной серной кислотой идет аналогично описанной выше реакции получения этилового эфира. Сначала образуется изоамилсерная кислота:
C5H11-OH + H2SO4 а C5H11-O-SO3H + H2O
Изоамилсерная кислота реагирует с другой молекулой спирта образуя эфир:
C5H11-O-SO3H + HO-C5H11 а C5H11-O-C5H11 + H2SO4
Изоамиловый эфир кипит при температуре, значительно превышающей ту, которая необходима для нормального хода реакции. Таким образом, удается избежать разбавления серной кислоты водой и добиться вступления в реакцию большей части взятого спирта. Довести реакцию до конца все же не удается, так как по мере накопления изоамилового эфира температура кипения смеси повышается и усиливаются побочные реакции, в частности разложение изоамилсерной кислоты с образованием изоамилена:
(CH3)2CH-CH2-CH2-O-SO3H а (CH3)2CH-CH=CH2 + H2SO4
Реактивы: 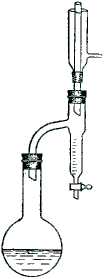 В круглодонной колбе (с не слишком длинным горлом) емкостью 200-250 мл смешивают свежеперегнанный изоамиловый спирт, кипящий в пределах 128-132°, с 4 мл концентрированной серной кислоты. При помощи корковых пробок колбу соединяют с насадкой для отделения воды и обратным холодильником (рис. 34). Смесь нагревают до кипения и слабо кипятят в течение нескольких часов до тех пор, пока в водоотделителе не соберется 9 мл (0,5 моля) воды.
Вначале перегонку ведут медленно. После отгонки небольшого количества амилена (кипящего при 21°) температура повышается и при 128° начинает отгоняться не вошедший в реакцию изоамиловый спирт. Когда термометр покажет 165°, меняют приемник, усиливают нагревание и в пределах 165-172° отгоняют изоамиловый эфир.
Выход около 50 г.
Продукт получается не вполне чистым. Для получения чистого эфира его кипятят с 1 г амида натрия, отгоняют, взбалтывают с разбавленной серной кислотой, сушат хлористым кальцием и перегоняют над металлическим натрием.
Темп. кип. 172°; уд. вес
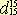 0,7807. 0,7807. Примером реакции получения простого эфира при действии галоидных алкилов на алкоголяты или феноляты может служить получение фенетола (фенилэтилового эфира):
C6H5-OH + C2H5-ONa а C6H5-ONa + C2H5-OH
C6H5-ONa + C2H5I а C6H5-O-C2H5 + NaI
Реакцию ведут в спиртовом растворе; спирт хорошо растворяет и фенолят натрия и иодистый этил, обеспечивая тем самым однородность среды и легкое протекание реакции.
Реактивы: В круглодонной колбе емкостью 100 мл, снабженной двугорлой насадкой и обратным холодильником, растворяют 2,3 г натрия в 30 мл спирта. Натрий вносят небольшими кусочками.
По охлаждении раствора к нему прибавляют фенол и иодистый этил и смесь нагревают на водяной бане до тех пор, пока спиртовый раствор не перестанет показывать щелочную реакцию. Затем колбу соединяют с нисходящим холодильником, отгоняют возможно полно спирт и прибавляют к остатку небольшое количество воды для растворения образовавшегося при реакции иодистого натрия.
Фенетол извлекают эфиром, эфирный раствор отделяют при помощи делительной воронки, взбалтывают с разбавленным раствором едкого натра для удаления не вступившего в реакцию фенола и сушат хлористым кальцием. Отгоняют эфир, заменяют водяной холодильник небольшим воздушным и при 167-172° перегоняют фенетол.
Выход около 9 г.
Фенетол - бесцветная жидкость с характерным запахом; темп. кип. 172°; уд. вес
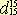 0,9702. 0,9702. |


