
   |
|
КНИГИ ПО ХИМИИ: |
|
|
При нагревании с водой органические галоидопроизводные, содержащие не более одного атома галоида у одного атома углерода, подвергаются гидролизу с образованием спиртов*1:
R-Hal + H2O а R-OH + HHal
Скорость с которой проходит гидролиз различных галоидопроизводных, неодинакова. Из соединений жирного ряда легче всего гидролизуются третичные галоидные алкилы; из ароматических соединений очень легко галоидопроизводные с атомом галоида в боковой цепи при атоме углерода, ближайшем к ядру. Напротив, галоид в ароматическом ядре очень трудно заместить на гидроксильную группу.
Гидролиз галоидопроизводных проходит значительно легче в присутствии оснований, связывающих образующуюся кислоту и создающих слабощелочную реакцию. Применение растворов едких щелочей приводит к усилению побочной реакции - образованию олефина с выделением галоидоводорода (за исключением, конечно, тех случаев, когда галоидосодержащая группа связана с третичным атомом углерода). К образованию непредельных соединений особенно склонны третичные галоидные алкилы.
Если гидролизу подвергается дигалоидопроизводное, в котором оба атома галоида находятся при одном атоме углерода, реакция приводит к образованию соответствующего альдегида или кетона. Гидролиз тригалоидопроизводных, содержащих 3 атома галоида при одном атоме углерода, приводит к образованию кислот.
Этиленгликоль образуется при гидролизе бромистого этилена согласно уравнению:
Гидролиз ведут в присутствии углекислого калия, нейтрализующего бромистоводородную кислоту и создающего слабощелочную реакцию раствора, способствующую ускорению процесса. В качестве побочного продукта реакции получается легколетучий (темп. кип. 16°) бромистый винил:
Реактивы: В круглодонную колбу емкостью 750 мл вливают 300 мл воды, прибавляют углекислый калий и бромистый этилен, присоединяют обратный холодильник и кипятят смесь в течение 20-30 час., нагревая колбу на воздушной или на песочной бане. Для уменьшения толчков при кипении в колбу бросают длинные, тонкие деревянные палочки, которые должны стоять в колбе вертикально.
Когда реакция закончится (о чем можно судить по исчезновению маслянистого слоя бромистого этилена), раствор упаривают в вакууме. Упаривание ведут в колбе Кляйзена емкостью 200 мл; взамен термометра присоединяют капельную воронку, через которую, по мере испарения жидкости в колбе, понемногу прибавляют новые порции раствора. Колбу погружают в водяную баню, нагретую до 50°.
Отогнав воду, дважды экстрагируют почти сухой остаток абсолютным спиртом (порциями по 25 мл). Спиртовые вытяжки соединяют и отгоняют спирт в вакууме из небольшой снабженной капилляром перегонной колбы (без термометра); отгонку спирта ведут на водяной бане, нагретой до 50°.
Остаток в перегонной колбе перегоняют при обыкновенном давлении, собирая три фракции: I - до 110°, II - от 110 до 170° и III - от 170 до 210°. Фракцию I отбрасывают, фракцию II перегоняют еще раз и дистиллят, переходящий в пределах 170-210°, присоединяют к фракции III, которую перегоняют вторично, собирая продукт, кипящий в пределах 190-200°.
Выход около 6 г.
Чистый этиленгликоль представляет собой густую жидкость с темп. кип. 197° уд. вес 1,109.
Гидролиз хлористого бензилидена является обычным техническим способом получения бензойного альдегида:
C6H5-CHCl2 + H2O а C6H5-C-H + 2HCl
Хлористый бензилиден обычно содержит примесь хлористого бензила и бензотрихлорида, дающих при гидролизе бензиловый спирт и бензойную кислоту. Особенно нежелательна примесь хлористого бензила, так как образующийся из него бензиловый спирт трудно отделить от альдегида. От бензойной кислоты освобождаются перегонкой альдегида с водяным паром из щелочной среды; для освобождения от других примесей переводят альдегид в бисульфитное производное.
Реактивы: В колбе емкостью 250 мл смешивают хлористый бензилиден, свободный от хлористого бензила (тщательной перегонкой должна быть удалена фракция, кипящая ниже 180°), с 0,1 г порошка железа и при перемешивании нагревают в течение получаса при 30°. Затем добавляют 5 мл воды и осторожно нагревают на водяной бане приблизительно до 100°, пока не начнется выделение хлористого водорода. В дальнейшем реакция продолжается сама собой без подогревания. Реакцию заканчивают кратковременным нагреванием колбы на водяной бане.
По окончании реакции прибавляют около 4 г углекислого натрия до ясно щелочной реакции по лакмусу и отгоняют бензойный альдегид с водяным паром. К отгону прибавляют 50-60 г бисульфита натрия, перемешивают и оставляют стоять на ночь. Маслянистый слой отделяют при помощи делительной воронки, а к прозрачной жидкости прибавляют растертый в порошок углекислый натрий в количестве, достаточном для полного разложения бисульфитного производного. Выделившийся альдегид отделяют при помощи делительной воронки, сушат небольшим количеством хлористого кальция и перегоняют.
Выход около 15 г.
Темп. кип. 178,1°; уд. вес
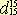 1,050; показатель преломления 1,050; показатель преломления  1,5456. 1,5456. Так как бензойный альдегид легко окисляется кислородом воздуха, все операции должны производиться быстро одна за другой.
К остатку в колбе после перегонки с водяным паром прибавляют при нагревании соляную кислоту до кислой реакции (по конго-рот) и фильтруют. Из фильтрата по охлаждении выпадает чистая бензойная кислота. Ее отсасывают, промывают небольшим количеством холодной воды и высушивают между листами фильтровальной бумаги.
Выход 2-2,5 г.
Темп. пл. 121,5°.
*1В уравнении реакции знак Hal обозначает атом галоида.
|


